在企业数字化办公持续深化的当下,私有化、
近日,一项发表于国际顶级期刊《Cell Metabolism》(IF=30.9)的突破性研究,首次揭示了一条“肠道微生物—免疫细胞—脂肪祖细胞”的全新信号轴。研究发现,寒冷环境可显著提升肠道普雷沃氏菌及其代谢物3-苯基丙酸(3-PPA)的水平,后者通过激活免疫细胞与祖细胞的“对话”,驱动米色脂肪生成,从而抵抗肥胖。这一发现不仅为代谢性疾病干预提供了全新靶点,更展现了高品质重组蛋白在复杂机制解析中的关键支撑价值。武汉云克隆(Cloud-Clone)重组CXCL13蛋白为本研究提供了核心验证工具。
从肠道到脂肪:一条全新的代谢调控通路
肠道菌群与能量消耗的关系一直是科学界探索的热点。此次研究给出了令人惊喜的答案。
研究团队首先证实,清除肠道菌群会显著削弱寒冷诱导的米色脂肪生成;而如果在肠道内定植一种名为普雷沃氏菌(P. copri) 的细菌,这一产热效应便能有效恢复。进一步代谢组学分析发现,P. copri能够高效合成小分子代谢物——3-苯基丙酸(3-PPA)。
外源补充3-PPA,可以精准模拟菌株定植带来的代谢获益:促进腹股沟白色脂肪组织(iWAT)发生“米色化”,提升小鼠的耐寒能力和能量消耗,且不影响经典棕色脂肪组织(BAT)的正常功能。
通俗理解:3-PPA就像一个“产热放大器”,寒冷是开关,它负责把信号放大,让白色脂肪转化为能够燃烧热量的米色脂肪。
靶点不是脂肪细胞,而是“脂肪干细胞”
有趣的是,3-PPA并不直接作用于成熟的脂肪细胞,而是优先靶向一类名为SMA⁺脂肪祖细胞(APCs)的“种子细胞”,驱动它们向米色脂肪细胞分化。谱系示踪实验明确证实,SMA⁺祖细胞是3-PPA诱导米色脂肪的主要来源。
在干预层面,寒冷环境下补充3-PPA可显著抵御高脂饮食诱导的肥胖与代谢紊乱。该效应严格依赖寒冷暴露,说明3-PPA是“放大器”而非“独立触发器”。更重要的是,这一机制在人脂肪祖细胞和猪模型中均得到了验证,展现出跨物种的转化潜力。
关键免疫桥梁:CXCL13如何连接代谢物与脂肪产热?
那么,3-PPA是如何“指挥”脂肪祖细胞的?机制解析带来了意外发现:3-PPA并不直接作用于祖细胞,而是先激活了一类M2样巨噬细胞。具体过程如下:
3-PPA与巨噬细胞上的FFAR1受体结合,增强其氧化磷酸化代谢,并诱导趋化因子CXCL13的分泌;CXCL13作为“信使”,招募CXCR5⁺滤泡辅助T细胞(Tfh) 浸润到白色脂肪组织;Tfh细胞分泌IL-4,激活SMA⁺祖细胞中的STAT6信号通路,最终促进米色脂肪生成。
这一回路构成了一个精妙的“免疫-祖细胞”协作网络:M2样巨噬细胞、Tfh细胞与SMA⁺祖细胞三者协同,打造出一个促米色化的免疫微环境。而CXCL13正是连接微生物代谢物与祖细胞活化的核心免疫介质。
精准工具的力量:重组CXCL13如何助力机制解析?
为明确CXCL13在米色脂肪生成中的功能,研究团队使用了高活性重组CXCL13(rCXCL13)开展系列验证。结果显示,在标准分化条件下,rCXCL13无法直接上调米色脂肪细胞中UCP1的表达——这排除了CXCL13直接作用于脂肪细胞的可能性,为后续机制溯源提供了关键依据。进一步实验表明(见图1):
rCXCL13显著提升iWAT淋巴结中CXCR5的表达;慢病毒敲低Cxcr5可完全阻断rCXCL13诱导的UCP1上调,证实CXCR5为必需受体;RNA-seq与流式细胞术证实,rCXCL13或3-PPA处理可选择性上调Tfh细胞标志物,并增加iWAT中CD4⁺Tfh细胞数量。共培养实验提供了决定性证据:仅在Tfh细胞存在时,rCXCL13才能促进米色脂肪生成;缺失Tfh细胞则完全失效。同时,rCXCL13特异性增强Tfh细胞分泌IL-4(而非IL-13)。
依托rCXCL13这一工具蛋白,研究团队清晰勾勒出 “CXCL13→Tfh细胞→IL-4→米色脂肪生成” 的完整信号链。
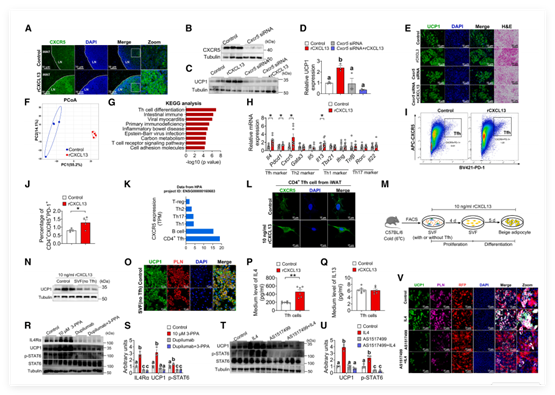
图1 CXCL13通过IL-4/STAT6信号通路招募并激活Tfh细胞,促进米色脂肪细胞的形成(图片来自《Cell Metabolism》)
研究启示:机制发现与工具应用的双重价值
本研究不仅揭示了3-PPA通过免疫-祖细胞对话调控米色脂肪生成的新机制,更凸显了高品质重组蛋白在解析复杂生理过程中的核心价值。rCXCL13的严谨应用,为区分直接/间接效应、鉴定靶细胞群、验证信号层级提供了不可替代的依据。
对于代谢、免疫与微生物组领域的研究者而言,选择高质量、高活性、经多重验证的重组蛋白,是决定机制探索深度与结论可靠性的关键环节。
云克隆:高品质重组蛋白,助力科研验证与转化应用
在CXCL13介导米色脂肪生成的机制验证中,武汉云克隆(Cloud-Clone)重组CXCL13蛋白(RPB601Mu01) 发挥了关键支撑作用。研究团队依托该高活性蛋白,严谨锚定了CXCL13→Tfh细胞→IL-4→米色脂肪生成信号轴,确立了CXCL13作为连接微生物代谢物与产热程序的核心免疫介质的地位。
武汉云克隆(Cloud-Clone)可提供:
超17,000种重组蛋白,覆盖人、小鼠、大鼠、猪等多物种;
蛋白表达、纯化与小分子抗原改造平台,依托生物反应器实现规模化生产,满足工业级需求;
超1,000种活性蛋白,涵盖细胞因子(TGF-β1、TNF-α、IL-2)、生长因子(GM-CSF、EGF)、酶类(过氧化氢酶、乙酰肝素酶、DNA聚合酶)及IVD靶标(AMH、PINP等);
严格活性验证:所有活性均经多重生物学实验验证,为基础研究与转化应用提供稳定可靠的工具支撑。
无论是前沿机制探索,还是诊断试剂与药物开发,云克隆致力于为全球科研工作者提供高可信度、高批次一致性的重组蛋白。
文章链接:
Cell Metab. 2026 Apr 7;38(4):763-778.e7.
doi: 10.1016/j.cmet.2026.01.017. Epub 2026 Feb 24.
*Microbial-derived 3-phenylpropionic acid orchestrates immune-progenitor cell crosstalk to promote beige adipogenesis and energy expenditure*
在企业数字化办公持续深化的当下,私有化、
摘要:随着生成式AI全面渗透搜索与内容分
4月17日,在数字中国建设峰会组委会指导
一、2026年RNA提取市场现状、行业趋
2025年,中国城镇犬猫数量已突破1.2
4月17日晚,青龙管业(002457)发
【2026年4月19日香港讯】随着全球人
近日,中国设计师珠宝品牌HEFANGJe
2026年一季度,博科电测(苏州)科技有
